Conocimiento sobre VIH/SIDA en las ciencias básica
Luis Soto
Introducción
La epidemia de VIH/SIDA ha impactado
al mundo no sólo por la magnitud del problema numéricamente
hablando, sino por una serie de factores colaterales entre
los que destacan el gran impacto en la mortalidad de sujetos
en edad productiva y reproductiva, la gran influencia sobre
la sexualidad humana y la apertura y conocimiento de conductas
y preferencias sexuales que con anterioridad se mantenían
en completo secreto.
Desde el punto de vista comercial,
se han hecho presentes todas las tendencias lucrativas de
las compañías farmacéuticas que viendo el gran campo de ventas
que los pacientes con VIH/SIDA representan, han invertido
sumas millonarias. Sin embargo, los resultados han sido en
buena manera decepcionantes y al momento actual cuando algunos
medicamentos son promisorios los gastos han sido ya tan altos
y/o los costos de producción tan elevados que dichos medicamentos
están fuera del alcance de la gran mayoría de los individuos
que los necesitan alrededor del mundo.
A nivel científico importantes cambios
se han dejado sentir. Un gran número de investigadores han
cambiado su campo de trabajo, y adaptando sus conocimientos
o técnicas se han movido al campo de VIH/SIDA, a donde se
han trasladado una importante proporción de los recursos económicos
destinados a la investigación básica. Con todos estos recursos
se han hecho una serie de descubrimientos en virología y biología
molecular sin precedente en la historia de la ciencia. Lo
que se ha llegado a conocer del Virus de Inmunodeficiencia
Humana a 13 años de su descubrimiento es sin duda más que
lo que se sabe de cualquier otro agente infeccioso. Paralelamente
al gran desarrollo científico obtenido, se ha creado una industria
de laboratorios que han pesto a disposición cualquier tipo
de equipos o reactivos para poder realizar investigación de
alto nivel, pero a precios excesivos.
Aún así, a 15 años del primer caso
de SIDA descrito en los Estados Unidos no hay un tratamiento
curativo ni una vacuna preventiva. Este hecho ha creado frustración,
desesperación e incertidumbre. Como consecuencia, no obstante
la magnitud cada vez mayor de la pandemia, se han recortado
los fondos destinados a la investigación y se ha perdido el
interés de los laboratorios y compañías farmacéuticas especialmente
para el diseño y prueba de candidatos de vacunas. Además,
esto ha creado una competencia por dichos fondos. En este
contexto, aún los considerados grandes personajes de la investigación
básica en VIH presentan ideas y conceptos que un año después
no tienen ya validez, y hacen que se ponga en tela de juicio
la ética de dichos investigadores.
Para los países en desarrollo incluyendo
América latina y el Caribe, esta situación de competencia,
ética dudosa y gran comercialización representa un predicamento,
especialmente en el desarrollo de la investigación básica.
Las preguntas que surgen al respecto son:
• Dados los pobres resultados
obtenidos en forma práctica en la investigación básica, ¿deben
invertir nuestros países en dicha investigación, o dedicar
los recursos a educación, prevención, diagnóstico oportuno
y/ o adquisición de nuevos medicamentos antivirales de alto
costo ?
• En caso de poder destinar
recursos para investigación básica, ¿a qué áreas de ésta se
les debe de dar prioridad y a cuáles no?
• Para establecer dichas prioridades
¿en qué información se debe confiar?
• Con objeto de mejorar las
perspectivas en este tipo de investigación,¿se deben establecer
colaboraciones con países en desarrollo ?
• ¿Quién o quiénes deben tomar
estas decisiones ?
En el documento que se desglosa a
continuación se hace una revisión actual de los conceptos
importantes en la ciencia básica relacionada a VIH/SIDA, con
los que se pretende llegar a responder por lo menos parcialmente
a las preguntas que hemos formulado.
Revisión previa a la XI Conferencia
Internacional sobre SIDA
Principales avances en el tema
Cuatro áreas en ciencia básica han
copado la mayor parte de los descubrimientos recientes en
relación a VIH/SIDA: los avances en el entendimiento de la
patogénesis especialmente a nivel de receptores y tropismo
celular; los hallazgos relacionados a nuevas estrategias terapéuticas;
el mejor entendimiento de la variabilidad genética de VIH
y, paralelamente, de la epidemiología molecular del virus,
así como las perspectivas a nivel de desarrollo de vacunas.
Recientemente se han descrito dos
receptores que actúan realmente como como co-receptores de
la molécula CD4. El primero es el denominado fusina que se
relaciona a la entrada de virus a líneas celulares de células
linfoides T(1). Por otro lado se describió un receptor de
las llamadas beta quimiocinas, que son citocinas que funcionan
como factores quimiotácticos de tipos celulares específicos,
denominado CC-CKR5 y el cual sirve como co-receptor para la
entrada de VIH-1 a macrófagos(2). Esto ha venido a explicar
parcialmente el efecto inhibidor de las beta quimiocinas secretadas
por los linfocitos CD8 descrito recientemente(3). Así, el
tropismo por tipos celulares específicos está determinado
tanto por factores del hospedero (célula) como del virus que
lo modifica con cambios sutiles o puntuales a nivel de las
áreas variables de la proteína de la cubierta (V1,V2 y V3),
y probablemente como consecuencia de la interacción múltiple
entre estas regiones(4). Las diferencias en tropismos de diferentes
virus se reflejan en varios aspectos de la patogénesis de
VIH pero importantemente en la transmisión. Así, las células
blanco a nivel genital (Langerhans) pueden determinar la selección
de ciertas variantes o subtipos(5) y esto a su vez determinar
la predominancia de dichas variantes virales en un determinado
grupo de riesgo.
Desde el punto de vista patogénico,
el cambio tan reconocido de fenotipo al inicio de las manifestaciones
clínicas de no formador a formador de sincicios pudiera explicarse
por un cambio en el receptor preferencial de CC-CKR5 a fusina(6).
Después de varios años de pobres
avances en la terapéutica de la infección por VIH ahora se
ha logrado incluso pensar en que la infección pudiera ser
erradicada o al menos inhibida por un largo período. Tres
factores han contribuido a estos avances, el mejor entendimiento
de la patogénesis, la disponibilidad de métodos cuantitativos
para medir la cantidad de RNA viral presente en plasma (carga
viral) y medicamentos más potentes.
La cuantificación de la carga viral
ha servido para medir el proceso de equilibrio y desequilibrio
entre la replicación viral y la disponibilidad de células
blanco y para caracterizar la magnitud y duración del efecto
antiviral de nuevos medicamentos(7). Por otra parte, la carga
viral parece estar claramente relacionada con la progresión
de la enfermedad (8,9).
La carga viral puede ser determinada
por varios métodos. Los primeros en ser usados fueron la determinación
de p24 y los cultivos cuantitativos. Ambos resultaron costosos
e inexactos. Actualmente tres métodos son los mas comúnmente
usados, todos ellos ya disponibles en forma comercial y todos
usando tecnología molecular de alto costo. Mediante transcripción
reversa de RNA (RT-PCR) en plasma se determina la cantidad
de éste en comparación con un estándar interno. Esta técnica
comercializada por Laboratorios Roche (Amplicor HIV Monitor
Test) es probablemente la mas sensible de todas y puede detectar
hasta 200 copias de RNA por ml. La amplificación de ácidos
nucléicos basada en secuencias o NASBA inicia, a semejanza
de la primera técnica, una transcripción reversa para luego
generar múltiples moléculas de RNA a partir del DNA obtenido,
las cuales son cuantificadas. Puede detectar hasta 400 copias
de RNA por ml. y está comercializada por Organon-Technika
(Q-NASBA). La tercera técnica no implica una amplificación
de ácidos nucléicos y es denominada b-DNA por “branched
DNA”. En este caso el RNA es fijado a una base sólida
y detectado mediante DNA con cadenas laterales que permiten
una detección colorimétrica. Esta técnica de baja sensibilidad
es comercializada por Chiron Corporation. Con cualquiera de
las técnicas, el costo aproximado es de 175 dólares americanos
para cada ensayo.
Los regímenes combinados de análogos
nucleósidos bajan la carga viral hasta 10 veces los valores
pre-tratamiento incluso hasta por 2 años, retardando pero
no previniendo la progresión(10). Los primeros resultados
con los nuevos inhibidores de proteasas, cuando se asocian
a análogos nucleósidos parecen reducir la carga viral mas
de 100 veces, por períodos de cerca de un año en 90% de los
pacientes tratados. Los niveles observados en tratamiento
por debajo de la capacidad de detección de las técnicas actuales
y por debajo de los niveles vistos en no progresores son muy
alentadores(11). Poco se conoce sin embargo del desarrollo
de resistencia en esas condiciones(12).
Es claro que actualmente hay indicación
para el uso de inhibidores de proteasas y de monitoreo con
carga viral, pero los costos de ambos son tan altos que se
calcula que en forma ideal solo 1 a 2% de los pacientes que
los requieren podrán usarlos en América latina y el Caribe.
La gran variabilidad genética observada
para VIH se ha relacionado claramente con la patogenicidad
del virus, el escape inmune y el desarrollo de resistencia
a antivirales. Sin embargo, su importancia se ha cuestionado
al descubrirse que la diversidad antigénica está inversamente
relacionada con la progresión a SIDA(13, 14). Este concepto
esta aún por ser corroborado puesto que existe amplia evidencia
que une la diversidad no sólo con la patogenicidad y desarrollo
de resistencia sino con otros fenómenos como la transmisión
diferencial de ciertos subtipos(5, 15, 16) .
La diversidad genética de VIH está
dada por dos acontecimientos muy importantes que son mutación
y recombinación, ambas ocurriendo a lo largo de un genoma
viral de 10,000 pares de bases. Las mutaciones son debidas
a la función incompleta de la enzima que replica el material
genético del virus o Transciptasa Reversa, la cual cuando
comete un error de copia es incapaz de repararlo. Se produce
aproximadamente una mutación por ciclo viral, lo cual al final
de 100 ciclos produce mutantes diversas. Por otra lado, la
recombinación es un acontecimiento aparentemente no-azaroso
que implica el intercambio de algunas regiones entre virus
de varios subtipos, lo cual origina variantes muy divergentes
en un solo ciclo. Es importante considerar que para una recombinación
entre subtipos, éstos deben coexistir en un mismo individuo(17,
18). La secuenciación de regiones específicas de gag y env
pueden ser un buen parámetro para evaluar las mutaciones pero
resulta incompleto para la recombinación, la cual requiere
de preferencia la secuencia de todo un genoma y de un proceso
de evaluación denominado ¨bootscanning¨. Hasta ahora sin embargo
solo existen 32 genomas virales secuenciados en su totalidad(19).
La variabilidad genética originada
ya sea por mutación o recombinación en las regiones de la
cubierta y de la cápside (gag), se traduce al momento actual
por la presencia de por lo menos 9 subtipos virales denominados
A hasta I, que se agrupan en una gran grupo M para diferenciarlo
de un grupo de secuencias muy distantes de cualquiera de los
subtipos y que no han podido clasificarse, al que se denomina
O (19-21). Los subtipos A hasta E presentan hasta el momento
una distribución geográfica característica donde A, C y D
dominan en Africa Sub-Sahara, C es predominante en India y
E en Tailandia. El subtipo B es el dominante en los Estados
Unidos y en Europa Occidental, en el Caribe y en América del
Sur. Virus subtipo B predominan en regiones geográficas donde
las vías de transmisión son principalmente a través de contacto
homosexual y de uso drogas intravenosas; en cambio subtipos
no B predominan en regiones donde prevalece la transmisión
heterosexual(19, 20). Poco se ha hablado de la traducción
biológica de estos subtipos. La única referencia proviene
de la replicación diferencial que existe en células de Langerhans
entre virus del subtipo E y el B. Como los posibles blancos
primarios de transmisión heterosexual a nivel genital son
Langerhans, el que repliquen mejor virus tipo E sugiere que
este tropismo pudiera ser la explicación a la expansión diferencial
de las epidemias B de drogadictos intravenosos y E de heterosexuales
en Tailandia, así como en otras localizaciones geográficas(5).
La transmisión heterosexual está
aumentando en todo el mundo y desde luego en América latina
y el Caribe. Aparte de Brasil, donde se han reportado virus
subtipo F y un reporte extraoficial de la Organización Mundial
de la Salud que revela la presencia de virus C en Honduras,
específicamente en San Pedro Sula, en donde epidemiologicamente
se ha detectado un brote de transmisión heterosexual, poco
es lo que se ha hecho en relación a subtipos en esta región
geográfica (22).
Finalmente, en los países desarrollados
occidentales es muy probable que otros subtipos aparezcan
y puedan ocasionar una epidemia de transmisión heterosexual.
Hasta el momento, sin embargo esto ha sido negado en Estados
Unidos y se ha empezado a probar en Europa.
En el campo de vacunas es importante
mencionar que ante las diferencias genéticas y biológicas
de los diferentes subtipos y la ausencia de reacción serológica
cruzada, se acepta que las vacunas deben de ser subtipo dirigidas,
lo cual acentúa más la necesidad de establecer los subtipos
virales predominantes en las diferentes regiones geográficas(23).
Una vacuna para VIH es la mayor esperanza
para controlar la pandemia especialmente en vista de los costos
de los tratamientos actuales y de la incertidumbre de su eficacia
a largo plazo. Las preguntas básicas para el desarrollo de
cualquier vacuna no han sido aún contestadas para VIH. Se
desconoce la respuesta inmunológica que tenga que crearse
y los antígenos virales más adecuados para producirla y finalmente
tampoco se ha creado un vector adecuado para liberar la vacuna
en el o los tejidos adecuados. En el momento actual están
a prueba más de 20 candidatos en estudios de fase I, y 2 o
3 candidatos en fase II, en ambos casos solo para seguridad
e inmunogenicidad, pero ninguno en fase III de eficacia(24,
25). Debido a que el número de individuos que se necesitan
para probar la eficacia de una vacuna se relaciona directamente
con la incidencia de la infecciones, es necesario llevar a
cabo los estudios de eficacia en países en desarrollo con
incidencias entre 6 y 16%(26). Sin embargo, a pesar de que
varios sitios se han preparado para estudios de eficacia (Brasil,
Tailandia, Uganda) no hay un consenso sobre si es adecuado
realizarlos, pues probablemente la protección sea muy baja
con los candidatos que existen actualmente .
Dos líneas de trabajo se han introducido
recientemente en el área de vacunas. Es posible introducir
DNA viral aislado en tejido muscular de animales y después
generar una respuesta inmune. Aún no se conoce si esta respuesta
es protectora, no se han hecho ensayos en humanos y existe
la duda de si secuencias integradas no pudieran causar la
aparición de neoplasias malignas(27).
Por otro lado, el uso de virus vivos
atenuados ha causado dudas. Aunque se cree pudiera ser efectivo,
no existen muchos estudios sobre formas adecuadas de atenuación
y, aún cuando existieran, es cuestionable si estos virus no
pudieran revertir a su original patogenicidad, al ocurrir
una superinfección, al recombinarse con secuencias retrovirales
en el genoma humano, y al ser transferidos a nonatos o a huéspedes
inmunocomprometidos(28, 29).
Principales preguntas de investigación
en el tema
Las preguntas que surgen de los avances
antes presentados son:
a) ¿Es la divergencia antigénica
de VIH originada en los diferentes receptores para su entrada
a las células?
b) ¿Cuáles son los epitopes del virus
y del receptor celular que interactúan?
c) ¿Cuál es el papel real de las
beta quimiocinas y de otras citocinas ?
d) ¿Son las técnicas actuales para
medición de carga viral adecuadas para todas las variantes
virales?
e) ¿Cómo pueden ser modificadas estas
técnicas para hacerlas de menor costo ?
f) ¿Qué medicamentos nuevos es posible
crear que sean efectivos y de bajo costo?
g) Los inhibidores de proteasa en
tratamiento, ¿serán capaces de erradicar la infección en sitios
santuario como los ganglios linfáticos?
h) ¿Cuáles son las consecuencias
de la gran disminución de carga viral de estos medicamentos
sobre la variabilidad viral y el desarrollo de resistencia?
i) ¿Existen otros subtipos virales
en los países desarrollados occidentales ?
j) ¿Cuáles son los subtipos prevalentes
en América latina y el Caribe ?
k) En caso de hallarse nuevos subtipos,
¿están estos asociados a transmisión heterosexual?
l) ¿Cuáles son los determinantes
virales de una mayor transmisión heterosexual?
m) ¿Es el tropismo por células de
Langerhans un fenómeno aplicable a otros subtipos o a variantes
del subtipo B?
n) ¿Se debe proceder con estudios
de eficacia (fase III) con algunos candidatos de vacunas y,
en dado caso, dónde?
o) ¿Cuáles son los parámetros inmunológicos
que se correlacionan con protección de una vacuna para VIH?
p) ¿Son seguras las vacunas de DNA
y de virus vivos atenuados?
Principales preguntas para el
proceso de toma de decisiones
Estas preguntas están parcialmente
delineadas en la introducción. Desde luego la más pertinente
para la América latina y el Caribe es: ¿Se debe hacer investigación
básica? Esta pregunta está en relación a los costos y al claro
liderazgo que los países desarrollados tienen en el área.
En caso de que la respuesta sea afirmativa, es necesario establecer
cuáles son las prioridades de investigación. Este proceso
debe de ser llevado a cabo por científicos que estén al día
de los nuevos descubrimientos y que tengan un amplio panorama
de la situación en la región. De cualquier manera, nuestros
alcances en ciencias básicas van a ser limitados, de modo
que es necesario preguntarse si sería conveniente establecer
colaboraciones con los países en desarrollo y en dado caso
con cuáles y en qué condiciones.
De todas las preguntas formuladas
en la sección previa, considero que la más importante para
América latina y el Caribe es la relativa a si se deben estudiar
los diferentes subtipos virales prevalentes en el área.
Revisión de la información presentada
en la XI Conferencia
Para esta revisión se consideró adecuado
conjuntar todos los puntos sugeridos para el folleto, por
lo que se han incluido los principales temas de investigación
revisados en la conferencia, aquellos importantes para la
toma de decisiones, mismos que están remarcados, los avances
temáticos de la conferencia y las mejores presentaciones (que
son mencionadas en las referencias con el número original
del resumen) así como algunos ejemplos negativos que deben
evitarse.
Nuevos métodos diagnósticos y
de seguimiento/pronóstico
a) Virológicos: Desde el punto de
vista virológico se presentaron hallazgos relativos a la cuantificacón
de carga viral así como de DNA proviral, extracción de genomas
completos para su completo análisis, cristalización de la
proteasa y desarrollo de la molécula SHIV.
En relación a la cuantificación de
carga viral es básica la utilización de un control de RNA.
Como el RNA es lábil y puede ser fácilmente degradado, se
presentó como alternativa el uso de RNA protegido para evitar
su degradación y se avaló su reproducibilidad(30) .
En vista de la diseminación de varios subtipos virales de
VIH-1 (véase la sección de conclusiones) es muy importante
que las técnicas de cuantificación viral de preferencia sean
útiles para todos los subtipos virales. A este respecto, en
el estudio L.B.A.6005, se presentó evidencia de que el equipo
comercial que utiliza la técnica de “branched DNA”
es capaz de detectar y cuantificar todos los subtipos de la
A a la F, mientras que el equipo que utiliza RT-PCR (Roche
Diagnostics Systems) no detectó muestras de subtipo A y por
otra parte que los valores obtenidos por esta técnica fueron
claramente menores para cepas E y F que en el equipo primeramente
mencionado(31). Ante esta información es muy importante que
las metodologías que se van a utilizar o a crear en América
latina y el Caribe sean dirigidas a los subtipos prevalentes
del área.
El construído viral SHIV es un retrovirus
simiano al cual se le han insertado los genes de la cubierta
(env), y de las regiones regulatorias tat y rev del VIH-1
y se ha visto que, inoculado intrarectalmente, intravaginalmente
y desde luego por vía intravenosa en simios, causa una rápida
caída de células CD4, por lo que es un modelo excelente para
probar la efectividad de candidatos a vacunas(32).
b) Inmunológicos: Desde el punto
de vista inmunológico se describió la posible importancia
de los receptores de quimiocinas, así como del factor CAF
(factor celular antiviral), la creación de nuevos vectores
basados en retrovirus y otros virus (caranarypox, adenovirus,
etc.), así como sistemas ex-vivo de expansión de células T
CD3+/CD28+, y métodos sencillos, rápidos y menos costosos
para la cuantificación de subpoblaciones de linfocitos.
c) Diagnósticos: Desde el punto de
vista de diagnóstico se describieron algunos nuevos sistemas
de ensayos inmunoenzimáticos (EIA), con especial énfasis en
la detección de virus grupo O, y se exaltó la técnica de mancha
de sangre seca (dried blot spot), con la cual se pueden realizar
en forma sencilla y confiable no sólo pruebas diagnósticas,
sino también determinación de subtipos virales(33).
En un nuevo acercamiento diagnóstico,
se presentó una técnica de aglutinación que utiliza como blanco
un péptido denominado TaBS, el cual fija la cubierta de VIH-1(gp120)
pero no la de VIH-2. Los resultados hasta el momento actual
son reproducibles en detección de virus provenientes de cultivos
celulares, pero no existen datos aún de su comportamiento
en suero o plasma(34).
Las tendencias futuras en ésta sección
de metodología deberán incluir prioritariamente el desarrollo
de técnicas de menor costo tanto para el diagnóstico como
para la determinación de carga viral. Por otra parte, deberán
crearse ensayos cuantitativos y reproducibles que evalúen
la respuesta inmune celular, así como estudiarse a fondo el
papel de los receptores de quimiocinas en la infección por
VIH y en la función inmune general.
Patogénesis de la infección por
VIH
Para que el VIH produzca daño del
sistema inmune y finalmente SIDA, se necesita la participación
conjunta de factores propios del virus y también del huésped.
Aun cuando los factores virales perecen tener un mayor peso
en este evento, en realidad es la interacción de ambos la
que da el resultado final.
Factores virales
La constante replicación viral es
probablemente la fuerza más importante que conduce a la inmunodeficiencia;
prueba de ello es que la cuantificación de la carga viral
es actualmente la guía básica del pronóstico de un individuo
infectado. La importancia de los factores virales se acentúa
además por el hecho de que el tamaño del inóculo inicial y
el fenotipo viral transmitido están directamente relacionados
con la rapidez de progresión a enfermedad.
En la replicación viral y concomitante
muerte celular de linfocitos CD4+, se mencionaron algunos
factores de importancia, como los que a continuación se consideran:
a) Entrada y transporte viral.
Una vez realizada la fusión de membranas (viral y celular),
el complejo de la nucleoproteína del virus es reconocido por
la célula a través de componentes celulares como la ciclofilina,
unión que trae como efecto final la liberación del contenido
genético viral(35). Poco después, una vez realizada la transcripción
reversa, el DNA proviral que resulta es transportado al núcleo
gracias a la interacción de la integrasa y acarreadores celulares
llamados carioferinas(36). Estos hallazgos abren más posibilidades
de blancos de terapia antiretroviral.
b) Replicación. En cuanto
a la replicación viral, los intentos por cuantificarla fueron
la novedad más relevante. Utilizando casos de infección por
VIH en hospederos específicos y a través e un mejor conocimiento
de la dinámica de las células linfoides, se ha calculado que
en un individuo infectado, se pueden producir 10 billones
de partículas en un día, de las cuales 200 a 700 partículas
provienen en forma aproximada de cada célula infectada(37).
Como consecuencia, en dicho individuo se originan 180 nuevas
generaciones virales por año. Esto es una clara explicación
de forma cuantitativa de la gran variabilidad viral, así como
de la facilidad con la que se desarrolla resistencia a los
diversos tratamientos antiretrovirales. Sin embargo, llama
la atención que estos conceptos probablemente tienen una utilidad
limitada tanto en la fisiopatogenia de la infección como en
el desarrollo de opciones terapéuticas, por lo que no se consideraron
prioritarios.
c) Infectividad. La infectividad
de VIH se ha relacionado con la presencia del producto del
gen regulador nef. Este producto actúa en conjunto con una
cinasa celular activando la transcriptasa reversa viral lo
cual ejerce un positivo efecto sobre la infectividad viral(38).
Por otra parte, se demostró que la proteína derivada del gen
nef es incorporada en los viriones, en donde es digerida en
dos porciones. Una de ellas, de aproximadamente 20 kilodaltons,
es la que se ha visto que ejerce el mayor efecto sobre la
infectividad de VIH-1. Este mecanismo podría explicar por
qué no ocurre progresión a enfermedad de individuos portadores
de VIH defectivos en el gen nef y por qué los inhibidores
de proteasa ejercen así mismo un efecto inhibidor de infectividad
al bloquear el desdoblamiento de nef en los viriones(39).
d) Dinámica Viral. Se pensaba
antes que el período asintomático de la infección por VIH
era un período de inactividad viral. En el momento actual
es claro sin embargo que consiste más bien de un estado de
equilibrio con una constante replicación viral y muerte celular
y con un reemplazo de células linfoides destruidas. En este
balance las fuerzas que mantienen el equilibrio son la respuesta
inmune y la disponibilidad de células blanco por un lado y
la replicación viral y la variabilidad genética viral por
el otro. Es en este contexto en el que los niveles de CD4
representan un parámetro de la distancia entre el estado actual
y la progresión a SIDA, mientras que la carga viral representa
la velocidad a la cual este cambio va a ocurrir(40).
Factores del huésped:
La importancia de los factores dependientes
del huésped queda claramente resaltada en la relación de la
respuesta inmune con la progresión de la enfermedad que ocurre
durante la infección primaria. En ese evento, la carga viral
no se correlaciona con la progresión pero sí con la presencia
de una respuesta inmunológica policlonal o monoclonal, en
relación al repertorio de receptores de las células linfoides
T(41). A continuación se mencionan otros factores que se consideran
relevantes:
a) Receptores. Aun cuando
el primer receptor descrito para VIH es el llamado CD4, parece
ahora claro que aparte de este receptor son necesarios algunos
otros factores celulares. Se mencionaron los dos co-receptores
del CD4 que fueron dados a la luz antes de la conferencia,
la fusina para los virus trópicos de células T y formadores
de sincicio(36) y CC-CKR5 para las variantes macrofago-trópicas(42).
Los linfocitos periféricos muy probablemente cuentan con ambos
co-receptores, mientras que los monocitos circulantes y los
macrófagos tisulares sólo portan CC-CKR5. No se mencionaron
sin embargo avances en la morfología o exacta función a nivel
estructural de estos receptores con respecto a su interacción
con VIH.
b) Tipos de células infectadas.
Aparte de las células blanco ya conocidas se describió la
infección de megacariocitos(43) así como de células mesangiales
del riñón(44). Estos hallazgos pudieran llegar a explicar
el porqué de la trombocitopenia asociada a VIH, así como del
daño renal descrito en individuos con esta infección. En el
caso de las células mesangiales, la infección activa la producción
de citocinas que pueden contribuir al daño renal.
c) Transmisión. En la transmisión
perinatal se ha visto que aparte de la ruptura de membranas
como factor de riesgo, es también de gran relevancia la excreción
viral a nivel genital. Esta excreción no se correlaciona con
niveles séricos de virus y pudiera estar dada por una producción
local originada en células infectadas como las de Langerhans
desde el momento de la transmisión del VIH a la madre o como
consecuencia de la infección. Este hallazgo puede tener relación
con la predominancia de fenotipo no formador de sincicios
en la infección primaria de los niños como consecuencia de
una producción preferencial de virus con este fenotipo a nivel
genital(45).
d) Función inmune. Poco es
lo que se conoce del verdadero efecto antiviral del aparato
inmune. En el momento actual muchos de los estudios están
enfocados a los efectos antivirales de las citocinas y especialmente
las quimiocinas.
La interleucina 1 alfa y 6, así como
el factor de necrosis tumoral son citocinas producidas abundantemente
en tejidos linfoides y las cuales inducen con potencia la
replicación de VIH. Este efecto positivo es a su vez inhibido
en presencia de IL-10 in vitro. Por otra parte, las beta-quimiocinas
como son RANTES y proteína inflamatoria de macrofagos (MIP
1 alfa y 1 beta) directamente disminuyen la replicación viral
en ciertos sistemas celulares in vitro(46). Este efecto ocurre
por otro lado a concentraciones mucho más elevadas de las
encontradas en el organismo. Aún cuando se ha demostrado que
las beta quimiocinas tienen efecto antiviral in vitro, in
vivo no se ha probado que se asocien con progresión de la
enfermedad ni con la carga viral por lo que su papel en el
control a largo plazo de la viremia es muy dudoso(47). Con
estos hallazgos es difícil creer que se haya propuesto utilizar
interleucina 10 inmediatamente en pacientes para ver su eficacia.
Este estudio, que prácticamente ha sido aceptado pues se originó
en una de las cabezas de la investigación en SIDA, se convierte
en uno de los más claros ejemplos negativos de toma de decisiones.
Otro factor que también afecta la
dinámica viral es el CAF (factor celular antiviral) producido
por células CD8+ y documentado especialmente en no-progresores
y en individuos de alto riesgo no infectados. No se ha podido
identificar que este factor pertenezca a alguna de las quimiocinas
conocidas aún cuando tiene un potente efecto inhibidor de
la replicación como ellas(48, 49). En los casos mencionados
donde la infección (replicación) se encuentra controlada,
existe aparentemente un equilibrio entre las células CD4+
y las CD8+ a través de producción de IL-2 por las primeras,
lo cual estimula a las CD8, que a su vez producen el CAF que
tiene como efecto inhibir la replicación viral (50).
La respuesta de las células T citotóxicas
en la infección primaria demostró un claro valor pronóstico
del curso de la infección. Cuando esta respuesta está deprimida
el pronóstico es siempre malo con rápida progresión.
El VIH por otra parte puede causar
directamente inmunosupresión . Este efecto está producido
por múltiples proteínas virales especialmente aquellas de
la cubierta (env) y aún por proteínas originadas en virus
defectivos y ocurre a través de muerte celular programada
o apoptosis. Las proteínas mencionadas estimulan las células
mononucleares de sangre periférica no infectadas a producir
una sustancia que es bloqueada por anticuerpos anti-linfotoxinas
pero no por -anti-fas o anti-IL-10 y que origina, al momento
en que la célula CD4+ se pone en contacto con el antígeno,
una muerte celular programada(51).
Tratamiento de la infección por
VIH
Los resultados presentados en esta
conferencia hablan claramente de la terminación de la época
de la monoterapia con zidovudina (ZDV). Por otra parte, se
corrobora la utilidad de iniciar el tratamiento en etapas
más tempranas, (200-500 células CD4+/ml) especialmente si
la carga viral es elevada, y la utilidad de combinaciones
de análogos nucleósidos (AZT/3TC, d4T/ddI y d4T/3TC). Probablemente
el mayor avance se encuentra en los resultados obtenidos con
los nuevos inhibidores de proteasas, los cuales en esquemas
combinados (AZT/3TC/Indinavir) disminuyen marcadamente la
carga viral incluso a niveles no vistos antes con otro tipo
de tratamiento (probable inhibición completa) y durante tiempos
prolongados (48 semanas). Estos aspectos que se revisan con
mayor énfasis en la sección clínica originan una pregunta
básica de la posibilidad de erradicación viral y curación.
Por ahora, se considera que el bloqueo de la replicación viral
pudiera ser sólo transitorio y no abarcar células fuera de
la circulación, por lo que la replicación viral reaparecería
al suspender el tratamiento. De cualquier manera si se prueba
que la inhibición pudiera ser de largo plazo, esto tendría
un gran impacto en aquellos individuos infectados. La búsqueda
de respuestas a estas interrogantes así como su repercusión
en la variabilidad viral, debe crear un campo especial de
investigación(40).
Se reafirmó el hallazgo de gran impacto
en la conferencia de Yokohama acerca de la protección del
tratamiento con ZDV a madre e hijo en la transmisión perinatal,
aunque ciertamente se avanzó muy poco en las repercusiones
que este tratamiento pudiera tener en cuanto a resistencia
y toxicidad(45). No se ha llegado a una conclusión acerca
de la dosificación y tiempo ideales de utilización de ZDV
en relación a efectividad, costo y efectos colaterales. Es
claro que el uso de una combinación de medicamentos y la inclusión
de inhibidores de proteasas, con mayor potencial de bloqueo
de replicación podrían mejorar la protección y disminuir importantemente
ó incluso impedir la transmisión perinatal.
El tratamiento con 3TC(lamivudina),
un análogo nucleósido incrementa la fidelidad de la enzima
transcriptasa reversa(52). Este efecto puede estar relacionado
o aumentado por la presencia de las mutaciones características
de resistencia a 3TC, especialmente Met184Val(53). Por lo
tanto, además de bloquear parcialmente la replicación viral,
la que no es bloqueada genera virus con menor heterogeneidad.
Para el futuro se deberá investigar
la seguridad y eficacia de nuevas combinaciones de tratamiento,
desarrollar nuevos prospectos tales como los inhibidores de
la enzima integrasa así como los inhibidores de tat/rev. Debe
evaluarse cuidadosamente en todos esos esquemas el verdadero
efecto de reducción de carga viral y las consecuencias de
ésta en la evolución de la enfermedad, y desde luego la aparición
de nuevas mutaciones asociadas a resistencia.
Desde el punto de vista inmunológico
se siguen estudiando tratamientos para restaurar la función
inmune. Dos acercamientos parecen altamente promisorios: uno,
el bloqueo de receptores de quimiocinas y dos, la expansión
in-vitro de células T no infectadas para poder ser reincorporadas
posteriormente al sujeto infectado en conjunto con inhibidores
de la replicación, que impidan que se infecten.
Pocos resultados se presentaron respecto
de la terapia génica y especialmente poco alentadores para
las ribozimas. Por otro lado, hay dos acercamientos nuevos
que pudieran ser promisorios. El primero inserta secuencias
de genes inhibitorios de replicación viral en células madre
linfoides que después pueden ser colocadas en pacientes infectados(54).
En el segundo se intenta la creación de nucleasas que sólo
tengan acción sobre RNA de VIH y que puedan ser transfectadas
en células humanas(55).
Resistencia a antiretrovirales
Aun cuando la causa mas común del
desarrollo de resistencia a antiretrovirales es la aparición
de mutaciones, la recombinación es un fenómeno que debe tomarse
en cuenta en especial al haberse documentado varios puntos
de recombinación a nivel de la polimerasa(56).
Las mutaciones y recombinaciones
existen ya al inicio de tratamiento y son seleccionadas al
mantenerse éste. Los eventos concomitantes en el desarrollo
de resistencia han servido para delimitar conceptos tales
como “viral fitness". Es claro que los virus salvajes
son más capaces de replicarse que los mutantes en ausencia
del antiretroviral (ZDV), pero esta relación se invierte en
presencia del medicamento (presión de selección, la cual aumenta
al aumentar el medicamento)(57). Esta clara diferencia en
“viral fitness” depende también del tipo celular
de que se trate; así, para mutantes del codón 84 su replicación
es mucho menor en z<células mononucleares de sangre periférica(CMSP)
que en líneas celulares T, por lo cual se recomienda usar
CMSP en todos los ensayos de dinámica viral de mutantes(58).
Este concepto de “viral fitness” influye también
en la continuación de la aparición de algunas mutaciones aún
después de suspender el medicamento(56), por las ventajas
replicativas que se presentan. Según este concepto, existen
claras diferencias en el desarrollo de resistencia entre los
medicamentos que tienen una limitada supresión de la replicación
viral (3TC), aquéllos con una moderada supresión (inhibidores
de proteasas) y los casos en que la supresión es completa
o casi completa (combinaciones dobles o triples). En este
último caso, el virus que podría volver a crecer si el tratamiento
se suspendiera sería el tipo salvaje y no mutantes(40).
Uno de los objetivos del tratamiento
es bloquear la resistencia, lo cual generalmente implica el
uso de al menos dos medicamentos, originando por un lado desarrollo
de resistencia para uno y por el otro, permanencia de cepas
no resistentes para el segundo. Esto muy probablemente se
relaciona con cambios en la estructura de la transcriptasa
reversa en el caso de los anE1 logos nucleósidos, tal
y como ocurre en presencia de las mutaciones 215 y 219 asociadas
a resistencia a ZDV (mutaciones supresoras). Las combinaciones
de ZDV con ddI o ddC, en contra de lo que se pensaba originalmente,
no bloquean el desarrollo de resistencia a ZDV. Por el contrario,
la combinación ZDV con 3TC en un paciente sin tratamiento
previo, origina la mutación I84V que confiere resistencia
a 3TC en forma lenta, bloqueándose el desarrollo de resistencia
a ZDV. En pacientes con tratamiento previo con ZDV, la resistencia
a 3TC se desarrolla rápidamente y se recobra la susceptibilidad
a ZDV.
La resistencia a inhibidores de proteasa
se asocia a mutaciones múltiples, algunas de las cuales pueden
ser específicas o comunes para otros compuestos del mismo
grupo. En el caso de Ritonavir e Indinavir, la mutación V82A
es básica para el desarrollo subsecuente de otras mutaciones,
de la misma manera que lo es la mutación L90M para Saquinavir.
En ocasiones, la sola presencia de esa mutación puede predisponer
al desarrollo de resistencia cruzada rápida cuando se cambia
de uno a otro inhibidor de proteasa. En estudios in vitro
se ha visto que para que ocurra un efecto aparente de disminución
de susceptibilidad a indinavir son necesarias al menos 3 mutaciones.
De cualquier manera, el efecto de gran supresión viral de
las combinaciones de análogos nucleósidos e inhibidores de
proteasa ha cambiado por completo la idea de resistencia,
en vista de que bajo esas condiciones es muy difícil que se
repliquen las variantes virales con mutaciones asociadas a
resistencia(59).
Vacunas en contra de VIH
El avance mas relevante en esta área
es el relacionado a la vacuna de DNA. Las dosis (cantidades
de DNA) necesarias se han podido disminuir gracias al uso
de lípidos catiónicos (vitamina D3) que favorecen la transfección
del DNA en las células del músculo esquelético(60). Se ha
demostrado ya la seguridad y respuesta inmune a estas vacunas
en roedores, conejos y primates, sin embargo es aún un aspecto
de preocupación la probable oncogenicidad, que no puede ser
descartada en un seguimiento corto de estos animales. Por
otro lado, se presentaron datos de protección en contra de
la infección por VIH en chimpancés que fueron vacunados con
DNA de la cubierta y de la región gag/pol. En ambos casos,
luego de que estos animales fueron retados en forma intravenosa,
han permanecido libres de infección de acuerdo a RT-CR hasta
26 semanas después del reto, mientras que los controles se
positivizaron a la segunda semana. Se han iniciado ya los
estudios fase I en humanos(61).
El trabajo que demuestra una protección
en contra de la infección por VIH en ratas, con el uso de
un anticuerpo monoclonal que neutraliza a aislados primarios
de múltiples subtipos (A a F), probablemente asociada a una
acción directa del anticuerpo en contra de una estructura
oligomérica nativa de gp120, debe tomarse con cautela, especialmente
en vista de los parámetros tan variables con los que se cuenta
para la evaluación de la neutralización y la poca extrapolación
de modelos ratones al humano(62).
Continúa un gran vacío por lo que
se refiere a cuáles son los parámetros inmunológicos que se
correlacionan con la protección. Hasta el momento parece ser
que las células T citotóxicas (CD8+, CD28-)tienen poco efecto
protector e incluso pudieran ser deletéreas, aún cuando se
siguen utilizando como parámetro de respuesta en candidatos
a vacunas. Por el contrario, los linfocitos CD8 no citotóxicos
(CD28+) parecen ser cruciales(50, 63). En el lado de inmunidad
humoral su importancia es poco reconocida aunque se ha corroborado
parcialmente que solo la neutralización homóloga está correlacionada
con protección. Nuevos ensayos con neutralización dirigida
a las regiones variables V1 y V2 de la cubierta y no a la
región V3 pudieran ayudar a resolver ésta deficiencia, según
los hallazgos sobre una variación marcada de la región V1
en relación a presión inmune(64).
Aún cuando no se ha dilucidado la
importancia de la inmunidad mucosa, poco es lo que se ha avanzado
para poder estimularla. Se presentaron datos de desarrollo
de anticuerpos en mucosas después de inoculación intranasal
de un esquema “prime-boost” con adenovirus como
vector y luego refuerzo con gp120 y con inoculación intra-rectal
aunque en ambos casos la respuesta sólo fue de IgG(65, 66).
Por el contrario, las nuevas vacunas de DNA producen una adecuada
respuesta mucosa y mediada por IgA(60).
Quedaron muchos aspectos por dilucidarse
al futuro. Es claro que todas estas vacunas deberán dirigirse
contra más de un subtipo, lo cual quedó demostrado en el trabajo
de Yamamoto y colaboradores(67) en que la protección de vacunas
con subunidades virales sólo fue subtipo específica, pero
a la vez se encontró que se puede inmunizar con dos subtipos
y encontrar protección contra ambos. Por otro lado, la mejor
respuesta inmune se ha obtenido con la técnica de “priming
and boosting”, es decir dar dosis iniciales de una vacuna
con vector reforzada por dosis subsecuentes de una sub-unidad
viral sola(68).
Es necesario contar con nuevos armas
de evaluación inmunológica cuantitativa y especialmente de
la rama celular para valorar el efecto de candidatos de vacunas.
Asimismo, se presentaron trabajos
que hablan de la efectividad de vacunas de virus vivos inactivados
en animales(69) pero no hubo mención de la posible reversión
a cepa patógena ni se presentaron modelos nuevos de inactivación
viral.
Con todos estos candidatos se deberán
crear nuevos ensayos de fases I y II en humanos. Es interesante
ver que los ensayos fase II no parecen asociarse a mayor frecuencia
de conductas de riesgo. Sin embargo, los casos de infecciones
concomitantes en estos ensayos no han sido estudiados completamente,
puesto que estas pruebas no estaban destinadas a valorar eficacia(70).
Lo que no ha quedado claro es si proceder con vacunas que
no tienen parámetros inmunológicos favorables a ensayos de
fase III de eficacia. Este aspecto fue muy debatido; para
las naciones en desarrollo con gran incidencia de infección
por VIH, una vacuna que diera una baja protección tendría
una repercusión muy importante tanto en costos como en sobrevida(71).
Esto argumento es válido si se considera que hasta el momento
no se ha avanzado en cuáles son los parámetros de protección,
para lo cual positiva o negativamente un ensayo de fase III
nos daría respuestas. Por otro lado, los recursos para estos
ensayos deben y van a ser originados en los países desarrollados
que son a su vez los que menos prisa tienen por iniciarlos(72).
Sea con uno u otro de los planteamientos, el consenso es que
se debe avanzar más rápidamente para evitar mayores consecuencias
de la pandemia.
Genotipos o subtipos internacionales
de VIH
La diversidad genética de VIH está
dada por eventos de mutación y recombinación. Se presentó
evidencia de cierta selección durante la recombinación. Se
ha visto que algunas secuencias son retenidas preferencialmente,
como lo es gp41 de virus subtipo A que está presente en virus
subtipo E, G, así como en las recombinantes A/D, sugiriendo
alguna selección para ese segmento(73). Es importante considerar
que para una recombinación entre subtipos, estos deben coexistir
en un mismo individuo. Se pensaba que esto era raro pero probablemente
no lo es tanto, especialmente en regiones geográficas donde
coexisten múltiples subtipos. Así, en Camerún se han documentado
infecciones dobles con VIH-1 y VIH-2 y con diferentes subtipos
del VIH-1 incluyendo grupo O e incluso se encontró un caso
de infección triple, el primero reportado(74).
De acuerdo a los 32 genomas virales
secuenciados en su totalidad se ha determinado que los que
son verdaderos subtipos son A, B, C y D, mientras que E y
G son recombinantes y para F, H, I y J aún no hay suficiente
información. Hasta el momento, 10% de todas las secuencias
reportadas son recombinantes, pero probablemente estas recombinantes
vayan a predominar en el futuro. Se han trazado claras avenidas
de recombinación que son esquematizadas a continuación:
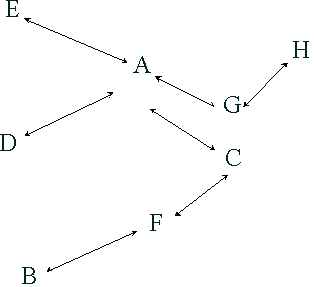
La distribución original que describía
subtipos muy bien localizados y limitados geográficamente
es cada vez menos válida. Aparte de que en el futuro las epidemias
podrían ser no sólo subtipo sino recombinantes específicas,
en está Conferencia ha quedado claro que existe una diversificación
y diseminación de subtipos y especialmente una considerable
expansión de subtipos no-B. Se describieron subtipos A, C,
D, F y G en Europa, F y C en Brasil y Argentina(75) y F y
D en México(76). Asimismo, en Nueva York (Bronx) 20% de los
subtipos encontrados fueron no-B, 5 subtipo A, 1 C, 1 B’
y uno no tipificable(77). Se describió el primer caso de infección
por grupo O en Estados Unidos. Aunque este caso probablemente
adquirió la infección en Africa Oeste, lo relevante es que
puede ser caso índice para otros individuos en los E.U.A.(78).
Se reportaron también infecciones por virus grupo O en 7 naciones
africanas que previamente no lo tenían. Esto último es de
gran importancia en vista de la dificultad que existe para
el diagnóstico de virus del grupo O(79) y sugiere la necesidad
de incorporar en los equipos diagnósticos péptidos específicos
para virus de ese grupo.
En general en América latina sigue
predominando el subtipo B, aunque es claro que existen ciertas
características particulares, como la presencia de la secuencia
GWGR en la corona de la región V3 tanto en Cuba(80) como en
Brasil(81). No se presentó ningún trabajo de tipificación
en Honduras. Sin embargo, en comunicación personal (Dr. Myron
Essex) los resultados obtenidos hasta ahora son muy semejantes
a los presentados para México con predominancia de virus B
y algunos D, que poseen importante homología con virus B.
Aparte de la gran importancia que
esto tiene para el desarrollo de vacunas adecuadas, la variación
viral se ha correlacionado con diferencias biológicas. En
esta conferencia se presentaron 2 trabajos que relacionan
ciertos fenotipos con subtipos virales. Las células de Langerhans
que son uno de los posibles blancos primarios a nivel genital
en transmisión heterosexual replican mejor virus subtipos
E (previamente ya publicado) y subtipo C que los B. Aunado
a esto se presentó clara evidencia que el receptor para el
VIH en estas células no es CD4. Este característico tropismo
pudiera ser la explicación a las diferencias en las epidemias
que se presentan en lugares donde predomina la transmisión
heterosexual(82). En apoyo de este hallazgo se presentó evidencia
de que en inoculación intravaginal de VIH en chimpancés, con
dosis infectantes similares en una mezcla de virus subtipo
E y B, 6 semanas después, todo el virus analizado de la sangre
de estos animales era subtipo E(83). Este factor y probablemente
otros se reflejan en lo ocurrido en Tailandia, donde en 1991,
en transmisión sexual 86% de los casos correspondían a subtipo
E y 14% a subtipo B y para 94-95 esto había cambiado a 98%
E y 0.7% B. Esto mismo se ha reflejado en cambios en los drogadictos
intravenosos en donde E representaba 24% en 91 y 44% en 94-95,
un fenómeno consecuencia de la gran predominancia del subtipo
E en la población(84, 85).
Por otra parte, la mayor transmisibilidad
de virus no B, hace pensar que otros subtipos podrían causar
una segunda epidemia en población heterosexual tal y como
ocurrió en Tailandia. Al respecto, en Bélgica se han descrito
recientemente virus A, C, D, F y H predominando en la población
heterosexual aunque en baja frecuencia probablemente relacionado
a una reciente introducción(86). Un fenómeno muy similar está
ocurriendo en Francia (F. Barin comunicación personal).
Asimismo, se estableció la importancia
de variantes asociadas a tipo de transmisión al identificar
a niños infectados de madres drogadictas , epidemiologicamente
no relacionados y con secuencias muy parecidas, lo que apoya
la presencia de una red social asociada indirectamente a través
de inyección de drogas(87).
Aún cuando el trabajo de Shioda y
colaboradores(88) demuestra mayor patogenicidad de virus subtipo
E que virus C, en este estudio aparecen diferencias en otras
características, como el fenotipo, que no apoyan sus conclusiones,
y en general la evidencia muestra que ninguno de los subtipos
es más patógeno sino sólo adaptado a ciertas vías de transmisión.
Por otro lado, es muy importante
la presencia de recombinación in vivo habiéndose reportado
virus que tienen partes de dos subtipos diferentes. Con esto
no parecen existir bordes geográficos pero sí muy probablemente
predominancia de subtipos o variantes de recombinación por
regiones o grupos de riesgo lo cual será de gran relevancia
en el diseño y aplicación de vacunas.
En un futuro es de esperarse, sin
embargo, que aparezcan más variantes. Esto ya se ha comenzado
a observar en sitios con gran dinámica de transmisión como
la India en donde el subtipo predominante C tiene ahora dos
variantes C2 y C3, la primera probablemente la más antigua
por la variabilidad genética que presenta y la segunda una
variante de probable reciente aparición(89). Esto puede explicar
por qué los resultados que han sido publicados en referencia
a la longevidad de la epidemia en la India son disímbolos.
Asimismo, el subtipo B que se encuentra en Tailandia es una
variante particular denominada B’ para diferenciarlo
del tradicional B de los Estados Unidos y Europa(84). Este
subtipo B’ se ha diseminado de Tailandia a la parte
sur de China que también ha recibido cepas subtipo C predominantemente
en drogadictos intravenosos(33) Birmania por otro lado ha
recibido ambos subtipos de Tailandia B’ y E(90).
Desde el punto de vista técnico,
vale la pena mencionar que a pesar de los buenos resultados
reportados con metodologías como serotipificación, “heteroduplex
mobility assay” y la hibridación con moléculas de DNA(91),
el estándar de oro para la tipificación viral es el secuenciamiento
y especialmente de regiones mayores de 1500 pares de bases.
Esto será mas relevante en la medida en que los subtipos se
vayan mezclando y sea más importante detectar secuencias específicas
relacionadas a ciertas características patogénicas.
Vacíos existentes en las áreas
bajo estudio
Problemas no tocados en la literatura
ni en la conferencia.
La información generada hasta el
momento de esta Conferencia ha resaltado la presencia y distribución
de varios subtipos de VIH. Sin embargo, algunos aspectos consecuencia
de esta información han sido pobremente referidos, u omitidos.
Aun cuando se ha incorporado en los equipos diagnósticos la
detección de virus grupo O, poco es lo que se ha dicho de
la efectividad de dichos equipos con otros subtipos y apenas
se ha comenzado a evaluar su repercusión en la cuantificación
de carga viral. Poco énfasis se ha puesto en la presencia
de infecciones dobles con dos subtipos diferentes de VIH-1
y solo dos trabajos han mencionado las importancia biológica
de dichos subtipos. Finalmente, aunque existe mucha información
de subtipos virales en diversas regiones del mundo, poca es
la información de América latina y el Caribe y especialmente
de Honduras en donde desde hace de una año se sospecha la
existencia de subtipos comunes en Asia. Aunque ya se encuentra
en proceso esta información de Honduras, obviamente originada
en instituciones americanas, llama la atención la falta de
interés de los Estados Unidos acerca de lo que ocurre endémicamente
en América latina y el Caribe, en vista de las corrientes
migratorias y de la descripción de subtipos no B en esas áreas,
que fácilmente pudieran llegar al país del norte.
Ha sido también sorprendente que
no se haya generado mas información de dos aspectos que en
la Conferencia de Yokohama fueron muy atractivos y que siguen
siéndolo. El primero es acerca de la transmisión materno-infantil,
que es un problema creciente a nivel mundial. Poco se ha avanzado
en cuanto a los mecanismos por los que ocurre, así como en
relación a los efectos adversos del tratamiento con Zidovudina.
El segundo es el aparente estancamiento de la información
generada por los individuos infectados no progresores y por
aquellos expuestos en múltiples ocasiones y no infectados.
A pesar de que en ellos está probablemente la respuesta de
los parámetros inmunes de protección contra la infección o
contra la enfermedad, prácticamente nada se ha avanzado al
respecto.
La ausencia de los parámetros inmunológicos
de protección ha retrasado mucho el campo de las vacunas.
Aún con nuevos candidatos muy atractivos llama la atención
la tibieza de los tomadores de decisiones para iniciar los
ensayos de eficacia. Por otra parte, la información generada
de los estudios de fase I y II no ha sido utilizada en su
totalidad, extrañando la ausencia de información acerca de
las infecciones concomitantes por VIH que han aparecido en
dichos estudios. Finalmente, y en vista de la gran importancia
que probablemente tenga la inmunidad mucosa, llama la atención
la falta de interés de algunos diseñadores de vacunas en ese
aspecto.
Conclusiones útiles para los tomadores
de decisiones
Los vacíos en investigación básica
de VIH/SIDA deben orientar a los tomadores de decisiones.
Para aquellos de los países desarrollados en los que se lleva
a cabo la mayor parte de dichas investigaciones, será importante
establecer políticas para el apoyo a proyectos de investigación
que tengan como objetivo cubrir áreas prioritarias olvidadas.
Estas áreas pueden determinarse en paneles de expertos que
deberán de llevarse a cabo en forma periódica. Para los tomadores
de decisiones en América latina y el Caribe estos ejemplos
deben servir para establecer una investigación básica coordinada
y no repetitiva, que esté orientada a aspectos prioritarios
como los mencionados en las conclusiones.
Conclusiones y recomendaciones
La ciencia básica aplicada a VIH
es uno de los campos menos explorados en América latina y
el Caribe, lo cual está en directa relación con los escasos
recursos destinados a esta rama y los altos costos que implica
su ejecución. Como clara evidencia, entre los trabajos presentados
en cualquiera de sus variedades en esta XI Conferencia Internacional
de SIDA solo 11 fueron originados en esta región geográfica
en el apartado A de investigación básica. Es interesante que
todos se referían a la tipificación de virus hecha en México,
Argentina, Brasil y Cuba.
Probablemente por esta limitación
sea difícil tomar decisiones en cuanto a políticas y acciones,
porque además de ser muy selectivas tienen que ser muy acertadas.
El avance más palpable hasta el momento
de esta Conferencia es desde luego el tratamiento combinado
con inhibidores de proteasa. Este tratamiento excesivamente
costoso, a decir de las compañías farmacéuticas por los elevados
costos de producción, es prácticamente inaccesible para la
gran mayoría de los individuos que por el grado de avance
de la infección por VIH más lo necesitan. Poco se puede hacer
para controlar los precios de estos medicamentos, pero, por
poco que sea, debe hacerse. Sería aconsejable disminuir impuestos
relacionados a esos productos y obtener precios ventajosos
para las instituciones de salud que los proveen. Aún así,
a un costo total aproximado de 80,000 pesos mexicanos por
paciente/año y con la necesidad de tratamiento por largo tiempo,
es poco probable que se pueda lograr una cobertura mayor.
El panorama se hace aún mas obscuro
cuando se toma en cuenta que para valorar este y cualquier
otro tipo de terapéutica es necesaria una prueba costosa como
es la carga viral. Este estudio permite no solo evaluar el
tratamiento sino establecer un pronóstico en cuanto a la progresión
de la enfermedad y por esas razones se convierte en prioritario
para ser puesto a disposición. Nuevamente, deben diseñarse
políticas que favorezcan la importación de los equipos utilizados
para la cuantificación de carga viral y su venta a precios
bajos. En este caso, sin embargo, contamos con otra posible
arma. Debe apoyarse la investigación para el desarrollo de
técnicas alternas o similares, pero hechas en casa, que desde
luego tengan un costo menor. Aún cuando esta misma conducta
se podría recomendar para la medición de linfocitos CD4, que
por ahora es utilizada para el pronóstico desde el punto de
vista clínico, además de que ya existen perspectivas de técnicas
más económicas, es claro que ante la superioridad de pronóstico
de la carga viral sea esta última la que deba apoyarse prioritariamente.
Con este panorama invadido por altos
costos, no hay duda que la mejor opción para el control y
prevención del VIH/SIDA es por el momento la educación y para
el futuro la posibilidad de contar con una vacuna preventiva
de bajo costo que pueda ser aplicada masivamente. Se debe
recalcar que no hay que perder de vista la educación para
la prevención porque ésta seguirá siendo un pivote en el control
de la epidemia aún con la vacuna, y especialmente si dicha
vacuna no fuera 100% protectora, lo cual es muy probable que
ocurra.
Por el momento se debe continuar
educando; no obstante, es necesario también tomar otras decisiones
que para un futuro serán de gran importancia. La primera de
ellas es la participación de países de América latina y el
Caribe en ensayos de eficacia (fase III) para candidatos a
vacunas. Creo que es claro que debemos participar en ellos
siempre y cuando haya una base sólida para su uso. Por otra
parte, debe ser también claro que de acuerdo al número de
casos nuevos que se presentan en esta región, ninguno de nuestros
países presenta el escenario adecuado para estos ensayos,
salvo una excepción. La razón básica es que entre menor sea
el número de casos nuevos mayor es el número de sujetos que
es necesario enrolar y mayor el tiempo para obtener una respuesta
de la efectividad del preparado en prueba. Así pues, parecen
mas adecuados países africanos y asiáticos como India y Tailandia
para estos ensayos y muy probablemente este último inicie
un ensayo de fase III este año o a principios del próximo.
La excepción es Brasil, que ha sido utilizado como blanco
por la Organización Mundial de la Salud para estudios de eficacia
y en el cual aparentemente se ha creado una infraestructura
adecuada, aunque poca es la información que apoya dicha afirmación.
Por otro lado, de acuerdo con la
información vertida referente a la variación genética del
virus y la presencia sin patrón específico de diversos subtipos
en diferentes regiones geográficas, cada país o al menos región
debe preparase para enfrentar la creación de una vacuna efectiva.
Si esta vacuna es como se ha mencionado subtipo dirigida,
es una prioridad establecer en América latina y el Caribe
las facilidades adecuadas para la óptima tipificación de aislados
de VIH. Y es necesario aclarar que óptima se refiere a las
siguientes consideraciones técnicas. Varias son las formas
en que se puede tipificar VIH, pero según los objetivos que
se establecen como prioridad, se debe realizar mediante secuenciación
nucleotídica de la región de la cubierta viral (env) de aislados
seleccionados, para tener una información completa de su variación
genética, especialmente de la región que está relacionada
con la entrada del virus a sus células blanco. Es claro que
la variación es cada vez mayor y que cepas específicas se
encuentran en algunos países o regiones, como es el caso de
la B’ en Tailandia. Hemos ya comentado que virus subtipo
D pero muy semejantes a los B han sido encontrados en México
y Honduras, y hasta ahora no descritos en otras regiones.
Además, no debemos olvidar que cuando hay dos o mas subtipos
en una región ocurre recombinación que a su vez origina la
aparición de nuevas variantes. El profundo conocimiento de
la información genética de nuestros aislados permitirá establecer
una respuesta adecuada ante una vacuna que pudiera ser efectiva
tal y como creada o modificada según las características particulares
de cada región o país.
Esta tipificación debe realizarse
en una forma orientada. Ya hemos visto que ciertos subtipos
tienen preferencia por vías específicas de transmisión, como
pudo corroborarse en uno de los trabajos mexicanos, por lo
que un minucioso estudio epidemiológico de grupos de riesgo
debe acompañar una selección de casos representativos de la
población para tipificación en vista de que técnicamente y
en costos es una metodología que no se puede aplicar masivamente.
Este hecho es claro en Honduras, donde se ha descrito una
epidemia de transmisión heterosexual y donde la Universidad
de Miami ha establecido un estudio epidemiológico inmejorable
del cual se han comenzado a tomar muestras para tipificación
en la Universidad de Harvard.
Estudios más sofisticados como el
tropismo o afinidad de ciertas variantes virales por células
blanco, como las de Langerhans en el tracto genital femenino,
deben también ser prioritarios porque ayudarán a la determinación
de factores patogénicos virales y del huésped particulares
de nuestra región.
Finalmente, no debemos olvidar que
hay que tener como prioridad el abarcar hasta la región mas
remota de nuestros países con un adecuado control de la sangre
y derivados que se van a utilizar clínicamente. Hoy por hoy,
existen aún un número considerable de casos de infección por
VIH originada en una deficiencia de la prueba diagnóstica
o una inadecuada realización de ella. Es necesario crear un
sistema que permita evitar esto, mediante una adecuada distribución
de equipos, entrenamiento del personal y vigilancia. Además,
debe insistirse en la utilización de equipos con un adecuado
control de calidad y que cubran todas las posibilidades de
subtipos virales presentes en el mundo. Es posible en este
ramo incentivar también la creación de equipos y reactivos
caseros de menor costo, pero que no sacrifiquen sensibilidad
ni especificidad y cuya calidad esté debidamente controlada.
Para finalizar, las respuestas concretas
a los planteamientos de nuestra introducción son: Sí se debe
invertir en investigación básica en VIH/SIDA en América latina
y el Caribe, pero con objetivos muy específicos. Entre las
áreas que se consideran prioritarias están el posible desarrollo
de técnicas mas económicas para el establecimiento del pronóstico
y el seguimiento del tratamiento de pacientes con VIH/SIDA
y para el adecuado diagnóstico de los portadores de dicha
infección y de los productos sanguíneos contaminados; la adecuada
tipificación de las variantes virales circulantes en la región;
y el estudio de los factores patogénicos de dichas variantes.
Para lograr esto es necesario que los tomadores de decisiones
se apoyen directamente en expertos en esta área básica, los
cuales deben estar actualizados así como crear una serie de
vínculos colaborativos con instituciones extranjeras prestigiadas,
siempre bajo términos de igualdad. Más importante aún es que
se fortalezca la comunicación entre los grupos que hacen investigación
básica en cada país y en cada región, a fin de evitar duplicidad
de funciones, un hecho común pero penoso en vista de los escasos
recursos.
Referencias
1. Feng Y, Broder CC, Kennedy PE,
Berger EA. HIV entry cofactor: functional cDNA cloning of
a seven-transmembrane G protein-coupled receptor. Science
1996;272:872-877.
2. Alkhatib G, Combadiere C, Broder
CC, Feng Y, Kennedy PE, Murphy PM. CC-CKR5: A RANTES, MIP-1alfa,
MIP-1beta receptor as a fisuon cofactor for macrophage-tropic
HIV-1. Science 1996;272:1955-1958.
3. Cocchi F. et al. Science 1995;70:1811.
4. Tsai WP, et al. AIDS Res Hum Retrovir
8, 1749(1992); Boyd M., et al. J Virol 37,3649 (1993); McKnight
A., et al. J Virol 69, 3167 (1995).
5. Soto-Ramirez LE, Renjifo B, McLane
MF, Marlink R., O’Hara C, Sutthent R., et al. HIV-1
Langerhans’ Cell Tropism Associated with Heterosexual
Transmission of HIV. Science 1996; 71:1291
6. Weiss R. A. HIV receptors and
the pathogenesis of AIDS Science 1996;272:1885-1886
7. Havlir DV and Richman DD. Viral
dynamics of HIV. Implications for drug development and therapeutic
strategies. Ann Intern Med 1996;124: 984-994.
8. O’Brien WA, Hartigan PM,
Martin D, Esinhart J, Hill A, Benoit S, et al. Changes in
plasma HIV-1 RNA and CD4+ lymphocyte counts and the risk of
progression to AIDS. N Engl J Med 1996;334:426-431.
9. Katzenstein TL, Pedersen C, Nielsen
C, Lundgren JD, Jakobsen PH, Gestoft J. Longitudinal serum
HIV RNA quantification: correlation to viral phenotype at
seroconversion and clinical outcome. AIDS 1996;10:167-173
10. C.C.J. Carpenter et al. J Am
Med Assoc In press.
11. Cao Y, Qin L, Zhang L, Safrit
J., Ho D.D. Virologic and Immunologic characterization of
long-term survivors of HIV type 1 infection. N Engl J Med
1995; 332:201-208.
12. Condra JH, Schleif WA, Blahy
OM, Gabryelski LJ, Graham DJ, Quintero C. In Vivo emergence
of HIV-1 variants resistant to multiple protease inhibitors.
Nature 1995;374:569-571.
13. Wollinsky SM, Korber BT, Neumann
AU, Daniels M, Kuntsman KJ, Whetsell A. Adaptative evolution
of Human Immunodeficiency Virus-type 1 during the Natural
Course of Infection. Science 1996;272:537-542.
14. Delwart EL, Sheppard HW, Walker
BD, Goudsmit J, Mullins JI. J Virol 1994;68:6672.
15. Miedema F. and Klein M.R.AIDS
pathogenesis: A finite immune response to blame?. Science
1996;272:505-506.
16. Nowak MA and Bangham CRM. Population
dynamics of immune responses to persistent viruses. Science
1996;272:74-79.
17. Mansky LM and Temin HM Lower
in vivo mutation rate of Human Immunodeficiency Virus type
1 than that predicted from the fidelity of purified reverse
transcriptase. J Virol 1995;69:5087-5094.
18. Moutouh L, Corbeil J, Richman
DD. HIV population dynamics in vivo: Implications for genetic
variation, pathogenesis and therapy. Proc Natl Acad Sci U.S.A.
In press; J.M. Coffin. Science 1995;267:483-489.
19. Siepel AC, Korber BT, En G. Myers,
B. Korber HIV Sequence Database, Los Alamos National Laboratory
1995; III-35.
20. Louwagie J, Janssens W, Mascola
J, et al. Genetic diversity of the envelope glycoprotein from
human immunodeficiency virus type 1 isolates of African origin.
J Virol 1995;69:263.
21. Weniger BG, Takebe Y, Ou C-Y,
Yamazaki S,. AIDS 1994;8:13s .
22. Esparza J, Comunicacion personal;
Informa de la Vigilancia del SIDA en América Central. Instituto
Latinoamericano de Prevención y Educación en Salud (ILPES),
Marzo de 1995.
23. Bloom BR. A perspective on AIDS
Vaccines. Science 1996;272:1888-1890.
24. Paul WE Can the immune response
control HIV infection?. Cell 1995;82:177-182.
25. Weiss R.A. Perspectives on retroviral
pathogenesis and vaccines. AIDS Res Hum Retrovir 1996;12:
465-467.
26. Martin HL Jr., Jackson DJ, Kisharchandra
M, Job B, Racwar JP, Nyonge P. Preparation for AIDS vaccine
evaluation in Mombasa, Kenya. Establishment of seronegative
cohorts of commercial sex workers and trucking company employees.
AIDS Res Hum Retrovir 1994;10: S235-S238.
27. Shiramizu B, Herndier BG, McGrath
MS Identification of a common clonal HIV integration site
in HIV-associated lymphomas. Cancer Res 1994;54:2069-2072.
28. Ruprecht RM, Baka TW, Liska V,
Bronson R, Penninck D, Greene MF. “Attenuated”
SIV in macaque neonates. AIDS Res Hum Retrovir 1996;12:459-460.
29. Desrosiers R.C. Safety issues
facing development of a live-attenuated multiply deleted HIV-1
vaccine. AIDS Res Hum Retrovir 1994;10:331-332.
30. Pasloske B, DuBois D, Winkler
M. Novel ribonuclease resistant RNA standards for HIV diagnostics.
XI International Conference on AIDS; 1996 julio 7-12; Vancouver,
Canadá. (Abstract LB.A. 6006).
31. Dunne AL, Crowe SM, Comparison
of branched chain DNA and RT-PCR for quantifying six different
HIV-1 subtypes in plasma. XI International Conference on AIDS;
1996 julio 7-12; Vancouver, Canadá. (Abstract LB.A. 6005).
32. Yichen L, Touzjian N, Kushner
N, Chutkowski C, Qian H., Jenkins S, et al. HIV-1 secreted
viral antigens (SVA), polyphosphazene adjuvant, and SHIV challenge
model. XI International Conference on AIDS; 1996 julio 7-12;
Vancouver, Canadá. (Abstract Mo.A.520).
33. Babu PG, Cassol S, Weniger BG,
Myo TH, Zheng X, Delaney A, et al. HIV-1 env subtypes A, B,
BB, C and E in dried blood spots (DBS) from China, India,
Indonesia, Myanmar (Burma) and Thailand. XI International
Conference on AIDS; 1996 julio 7-12; Vancouver, Canadá. (Abstract
We.C.340).
34. Yokohama H, Hamamoto H, Fujii
T, Otake T, Mori H., Kawahata T, et al. A new approach to
HIV diagnosis: HIV can be detected directly. XI International
Conference on AIDS; 1996 julio 7-12; Vancouver, Canadá. (Abstract
Th.A.4046).
35. Zybarth G, Dubrovsky L, Bucala
R, Ulrich P, Rich D, Cerami A, et al. Cyclophilin mediates
early events in HIV-1 life cycle via interaction with a putative
cyclophilin receptor. XI International Conference on AIDS;
1996 julio 7-12; Vancouver, Canadá.(Abstract LB.A. 6003).
36. Trono D. Molecular mechanisms
of HIV infection: viral factors and cellular accomplices.
XI International Conference on AIDS; 1996 julio 7-12; Vancouver,
Canadá. (Abstract We.11).
37. Goudsmit J, De Wolf F, Lukashov
VV, Van Oers RHJ, Bakker M, Boucher CAB, Danner SA. In vivo
evidence for modulation of HIV-1 dynamics by target cell availability
and cellular immunity. XI International Conference on AIDS;
1996 julio 7-12; Vancouver, Canadá. (Abstract Mo.A.382).
38. Trono D. The multifaceted role
of nef in HIV replication. XI International Conference on
AIDS; 1996 julio 7-12; Vancouver, Canadá. (Abstract Tu.A.490).
39. Miller MD, Warmerdam MW, Benitez
B, Greene WC. HIV-1 nef enhancement of viral infectivity is
correlated with its incorporation into virions and its cleavage
by the HIV-1 protease. XI International Conference on AIDS;
1996 julio 7-12; Vancouver, Canadá. (Abstract Th.A.921).
40. Coffin JM. HIV viral dynamics.
XI International Conference on AIDS; 1996 julio 7-12; Vancouver,
Canadá.Abstract Th.18.
41. Pantaleo G. Role of host factorsin
the resistance to intracellular pathogens. XI International
Conference on AIDS; 1996 julio 7-12; Vancouver, Canadá. (Abstract
Th.20).
42. Deng H, Liu R, Ellmeier W, Choe
S, Unutmaz D., Burkhart M., et al. Identification of C-C chemokine
receptor 5 as the major coreceptor for entry of macrophage
tropic human immunodeficiency virus type 1. XI International
Conference on AIDS; 1996 julio 7-12; Vancouver, (Canadá. Abstract
Th.A.927).
43. Chelucci C, Federico M, Guerreiro
R, Pelosi E, Testa U, Hassan HJ., Peschle C. Productive human
immunodeficiency virus infection of highly purified megakaryocytic
precursors and mature megakaryocytes. XI International Conference
on AIDS; 1996 julio 7-12; Vancouver, Canadá. (Abstract TuA.2043).
44. Toniolo A, Conaldi PG, Biancone
L, Mossa A, DeMartino A, Falcone V, Serrra C, Camussi G. Effects
of HIV-1 and viral glycoproteins on glomerular and tubular
renal cells. XI International Conference on AIDS; 1996 julio
7-12; Vancouver, Canadá. (Abstract TuA.2044).
45. Bryson YJ. Perinatal tranmsmission:
associated factors and therapeutic approaches. XI International
Conference on AIDS; 1996 julio 7-12; Vancouver, (Canadá.Abstract
Tu.07).
46. Fauci A. Host factors in the
pathogenesis of HIV disease. XI International Conference on
AIDS; 1996 julio 7-12; Vancouver, Canadá. (Abstract TuB.290).
47. Asher MS, Krowka J, Gesner M,
Sheppard H. Lack of association of chemotactic cytokines with
viral burden, disease progression or lymphocyte subsets in
HIV disease. XI International Conference on AIDS; 1996 julio
7-12; Vancouver, Canadá. (Abstract Th.A.924).
48. Levy JA, Mackewicz C, Barker
E, Strandford S. Chemokines and HIV infection. XI International
Conference on AIDS; 1996 julio 7-12; Vancouver, Canadá. (Abstract
Tu.A.503).
49. Levy JA.Challenges of HIV research
as we approach the 21st century. XI International Conference
on AIDS; 1996 julio 7-12; Vancouver, Canadá. (Abstract TuB.291).
50. Levy JA, Blackbourn DJ, Barker
E, Mackewicz C, Stranford S. HIV variability and host control
in HIV pathogenesis. XI International Conference on AIDS;
1996 julio 7-12; Vancouver, Canadá. (Abstract We.A.500).
51. Shearer GM Antigenic-stimulated
apoptotic T cell death: a model for CD4+ cell depletion in
HIV-1 infection. XI International Conference on AIDS; 1996
julio 7-12; Vancouver, Canadá. (Abstract We.A.501).
52. Wainberg MA, Hsu M, Gu Z, Inouye
P, Quan Y. Enhanced fidelity of 3TC-selected M184V HIV reverse
transcriptase. XI International Conference on AIDS; 1996 julio
7-12; Vancouver, Canadá. (Abstract Mo.A.380).
53. Prasad VR, Drosoppoulos W. Mutations
associated with 3TC-resistance enhance the polymerase fidelity
of HIV-1 RT. XI International Conference on AIDS; 1996 julio
7-12; Vancouver, Canadá. (Abstract Mo.A.381).
54. Junker U, Plavec I, Bonyhadi
M, Baker J, Kaneshima H., Bonhlein E. Hematopoietic Stem Cell
Based gene Therapy for AIDS. XI International Conference on
AIDS; 1996 julio 7-12; Vancouver, Canadá. (Abstract LB.A.6002).
55. Sadhna J, Melekhovets YF. “Designer
nucleases” with HIV-1 RNA specificity and their use
in anti-HIV-1 gene therapy. XI International Conference on
AIDS; 1996 julio 7-12; Vancouver, Canadá. (Abstract LB.A.6011).
56. Mayers D. The evolutionary biology
of HIV drug resistance. XI International Conference on AIDS;
1996 julio 7-12; Vancouver, Canadá. (Abstract Mo.A.385).
57. Harrigan PR, Bloor S, Nowak M,
Larder BA. Retroviral fitness and drug selection pressure.
XI International Conference on AIDS; 1996 julio 7-12; Vancouver,
Canadá. (Abstract Mo.A.383).
58. Boucher C. Reduced replication
rate conferred by mutations at codon 184 in peripheral blood
mononuclear cells. XI International Conference on AIDS; 1996
julio 7-12; Vancouver, Canadá. (Abstract Mo.A.384).
59. Emini EA, Condra JH, Schleif
WA, Massari FE, Leavitt RY, Deutsch PJ, Chodakewitz JA. Maintenance
of lon-term virus suppression in patients treated with the
HIV-1 protease inhibitor Crixivan (Indinavir). XI International
Conference on AIDS; 1996 julio 7-12; Vancouver, Canadá. (Abstract
Mo.B.170).
60. Mitchell W, Ding L, Baird C.
Induction of mucosal and systemic immune response to HIV gp
160 by genetic vaccination. XI International Conference on
AIDS; 1996 julio 7-12; Vancouver, Canadá. (Abstract We.A.390).
61. Boyer JD, Ugen KE, Wang B, Bagrazzi
M, Chatergoon M, Javadian A, Ciccareli R, et al. Induction
of ptotection from HIV-1 challenge in chimpanzees by DNA vaccination.
XI International Conference on AIDS; 1996 julio 7-12; Vancouver,
Canadá. (Abstract Th.A.923).
62. Parren PWHI, Fiscaro P, Barbas
CF., Burton DR. Inactivation of HIV-1 by recombinant antibodies.
XI International Conference on AIDS; 1996 julio 7-12; Vancouver,
Canadá. (Abstract Mo.A.264).
63. Barker E, Bossart KN, Fujimura
S, Levy JA. Ability of CD8+ cells to suppress HIV replication
is dependent on the presence of cells expressing the CD28
molecule. XI International Conference on AIDS; 1996 julio
7-12; Vancouver, Canadá. (Abstract Th.A.101).
64. Wei L, Andrieu JM. Evidences
for an immune selection pressure on the first hypervariable
region of HIV-1 and HIV-2 env genes in vivo. XI International
Conference on AIDS; 1996 julio 7-12; Vancouver, Canadá. (Abstract
Tu.A.512)
65. Buge S, Lubeck M, Kalyan N, Cheng
S, Richardson RE, Markham P, Miller C, et al. Adenovirus host
range mutant-SIV recombinant vaccine trial in Rhesus macaques.
XI International Conference on AIDS; 1996 julio 7-12; Vancouver,
Canadá. Abstract Mo.A.102.
66. Polacino P, Stallard V, Klaniecki
J, Brown C, Watanabe R, Morton WR, et al. Immunization with
SIVmne envelope (gp160) vaccines protected macaques against
intrarectal challenge by uncloned virus. XI International
Conference on AIDS; 1996 julio 7-12; Vancouver, Canadá. (Abstract
Mo.A.103).
67. Yamamoto JK, Mison M, Elyar JK,
Tellier MC, Pu R. Efficacy evaluation of conventional dual-subtype
HIV vaccine. XI International Conference on AIDS; 1996 julio
7-12; Vancouver, Canadá. (Abstract Mo.A.101).
68. Clemens Ml, Weinhold K, Siliciano
R, Schwartz D, Mattews T, Graham B, et al. HIV immunity induced
by canarypox (ALVAC)-MNgp160,SF-rgp120 or both. XI International
Conference on AIDS; 1996 julio 7-12; Vancouver, Canadá. (Abstract
Mo.A.281).
69. Addawe MD, Fabrizzi F, Dormashkin
R, Wilson S, John S. Cehmically inactivated whole HIV vaccine
induces cellular responses in mice. XI International Conference
on AIDS; 1996 julio 7-12; Vancouver, Canadá. (Abstract Mo.A.100).
70. McElrath MJ, Montefiori D, Wolff
M, Clements M, Gorse G, Keefer M, et al. Safety, immunity
and risk behaviour in HIV-1 uninfected volunteers representing
diverse risk populations following recombinant envelope vaccinations:
a three year followup. XI International Conference on AIDS;
1996 julio 7-12; Vancouver, Canadá. (Abstract Mo.A.284).
71. Mbidde E. HIVvaccines: resolved
that more fundamental research on vaccine development is required
prior to the implementation of phase III trials of HIV vaccines.
XI International Conference on AIDS; 1996 julio 7-12; Vancouver,
(Canadá. Abstract Tu.10)
72. Moore JP. HIV vaccines: resolved
that more fundamental research on vaccine development is required
prior to the implementation of phase III trials of certain
HIV vaccines. XI International Conference on AIDS; 1996 julio
7-12; Vancouver, Canadá. (Abstract Tu..09).
73. McCutchan FE. HIV genetic diversity.
XI International Conference on AIDS; 1996 julio 7-12; Vancouver,
Canadá. (Abstract Mo.02).
74. Takehisa J, Zekeng L, Miura T,
Ido E, Yamashita M, Mboudjeka I, et al. Phylogenetic analysis
of HIV 1/2 in Cameroon based on the pol and env regions:evidence
of mixed infection. XI International Conference on AIDS; 1996
julio 7-12; Vancouver, Canadá. (Abstract TuA.372).
75. Fay FF, Campodonico M, Taborda
M, Janssens W, Heyndrickx L, Fay Q. Prevalence of HIV-1 subtypes
in Argentina in different risk groups. XI International Conference
on AIDS; 1996 julio 7-12; Vancouver, Canadá. (Abstract TuA.373).
76. Soto-Ramirez LE, Renjifo B, Marlink
R, Essex M. Mexican HIV-1 V3 loop sequences grouped according
to route of transmission. XI International Conference on AIDS;
1996 julio 7-12; Vancouver, Canadá. (Abstract TuA.2081).
77. Irwin KL, Pu CP, Hu D, Lupo D,
Schable CA, Olivo N., Minor P., et al. Unusual HIV serotypes
in the Bronx community with high HIV prevalence: a sentinnel
site for monitoring HIV genetic diversity in North America.
XI International Conference on AIDS; 1996 julio 7-12; Vancouver,
Canadá. (Abstract We.C.345).
78. Sullivan PS, Simon P, Ward JW,
Britvan L, Gould K, Dryjanski J, et al. Identification of
group O HIV infection in the United States. XI International
Conference on AIDS; 1996 julio 7-12; Vancouver, Canadá. (Abstract
Th.A.922).
79. Saragosti S, Loussert-Ajaka I,
Mauclere P, Descamps D, Bouchaud O, Simon F, Brun-Vezinet
F. Genotypic and phenotypic charracterization of HIV-1 group
O strains. XI International Conference on AIDS; 1996 julio
7-12; Vancouver, Canadá. (Abstract TuA.371).
80. Gomez CE, Iglesias E, Fernandez
J, Lobaina L, Noa E, Diaz H, et al. DNA sequence of the C2-V3
region of the external glycoprotein (gp120) from Cuban HIV-1
infected individuals. XI International Conference on AIDS;
1996 julio 7-12; Vancouver, Canadá. (Abstract TuA.2057).
81. Casseb J, Hong M Gonsalez C,
Duarte A, Hendry RM. HIV-1 serotyping among a cohort of individuals
from Sao Paulo city, Brazil. XI International Conference on
AIDS; 1996 julio 7-12; Vancouver, Canadá. (Abstract TuA.2082).
82. Soto-Ramirez LE, Renjifo B, Marlink
R, McLane MF, Essex M. Differential growth of HIV-1 in Langerhans’
cells. Relation to transmission route. XI International Conference
on AIDS; 1996 julio 7-12; Vancouver, Canadá. (Abstract TuA.370).
83. Girard M, Barré-Sinoussi F, Tartaglia
J, Van der Ryst E, Paoletti E, Nara P., et al. Immunization
with an HIV-1 Canarypox virus recombinant confers protection
against genital HIV-1 challenge in chimpanzees. XI International
Conference on AIDS; 1996 julio 7-12; Vancouver, Canadá. (Abstract
We.A.393).
84. Subbarao S, Limpakarnjanarat
K, Bhumisawasdi J, Young NL, Kalish ML, Schochetman S, Mastro
TD. Genetic diversity od HIV-1 in Thailand 1994-1995. XI International
Conference on AIDS; 1996 julio 7-12; Vancouver, Canadá. (Abstract
TuA.375).
85. Mastro T, Ungchusak K, Vanichseni
S, Young N, Limpakarnjanarat K, Raktham S, et al. The evolution
of HIV-1 subtypes B and E in heterosexuals and injecting drug
users (IDUS) in Thailand 1992-1995. XI International Conference
on AIDS; 1996 julio 7-12; Vancouver, Canadá. (Abstract We.C.342).
86. Fransen K, Buv A, Nkengasong
J, Janssens W, Heyndrickx L, Colebunders R, et al. The distribution
of HIV-1 subtypes in the Belgian population. Europe is different
from the United States of America. XI International Conference
on AIDS; 1996 julio 7-12; Vancouver, Canadá. (Abstract We.C.343).
87. Kalish ML, Wiener P, Nesheim
S, Lee F, Meadows L, Grimes V, et al. Detection of phylogenetically
linked HIV strains among a population of epidemiologically
unrelated women. XI International Conference on AIDS; 1996
julio 7-12; Vancouver, Canadá. (Abstract TuA.2078).
88. Shioda T, Oka S, Xin X, Liu H,
Harukuni R, Fukushima M, et al. V2 extension of HIV-1 associated
with slow/moderate disease progression. XI International Conference
on AIDS; 1996 julio 7-12; Vancouver, Canadá. (Abstract TuA.2066).
89. Gadkari DA, Moore D, Sheppard
H, Mehendale S, Kulkarni S, Bollinger R. Viral subtype analysis
of HIV-1 infected patients from Pune, India. XI International
Conference on AIDS; 1996 julio 7-12; Vancouver, Canadá. (Abstract
TuA.374).
90. Shao Y, Zhao Q, Guan Y, Zeng
Y, Chang J, Koestler J. Wolf H. Follow-up studies on molecular
epidemiology of HIV-1 strains in Ruili region of southwest
China. XI International Conference on AIDS; 1996 julio 7-12;
Vancouver, Canadá. (Abstract We.C.341).
91. Luo CC, Downing R, De la Torre
N, Candal D, Hu D, Otten R.A., et al. The evaluation of probe
hybridizarion method used for the large scale screen of the
distribution of HIV in Uganda. XI International Conference
on AIDS; 1996 julio 7-12; Vancouver, Canadá. (Abstract We.C.344).
|